化学療法誘発性末梢神経障害(CIPN)は、抗がん剤治療に伴う一般的な副作用であり、末梢神経がダメージを受けることで発症します。主な症状としては、手足のしびれ、痛み、感覚異常、筋力低下などが挙げられます。これらの症状は、抗がん剤治療中だけでなく、治療後も長期間持続することがあります。CIPNの発症リスクは、使用する薬剤の種類や投与量、治療期間、患者の年齢、既存の神経障害の有無などによって異なります。特に、糖尿病やアルコール依存症などの既存の末梢神経障害を持つ患者では、CIPNのリスクが高まるとされています。CIPNを引き起こす主な抗がん剤には、タキサン系(パクリタキセル、ドセタキセル)、プラチナ製剤(シスプラチン、オキサリプラチン)、ビンカアルカロイド系(ビンクリスチン、ビンブラスチン)、プロテアソーム阻害剤(ボルテゾミブ)などがあります。現在のところ、CIPNの予防や治療に関して確立された方法は限られています。一部の研究では、冷却療法や圧迫療法の有効性が報告されていますが、これらの方法がすべての患者に適用できるわけではありません。また、薬物療法としては、抗うつ薬や抗けいれん薬の使用が検討されていますが、その効果は限定的であり、副作用のリスクも考慮する必要があります。近年、CIPNに対する新たな治療法の研究が進められており、その中にはカンナビノイド療法の可能性も検討されています。
CIPNの治療手段としての大麻への関心は、カリフォルニア州のエイズ患者における神経障害性疼痛の管理における有効性に関する初期の観察結果に端を発します。1980年代から1990年代にかけて、メアリー・ジェーン・ラスバン(通称「ブラウニー・メアリー」)のような人々が、痛みや食欲減退などの症状を緩和するために、大麻入りのブラウニーをサンフランシスコのエイズ患者に配るなどの自己治療を展開しました。患者たちが経験したとされる様々な効能は、大麻の潜在的な治療用途に大きな注目を集めることとなったのです。
こうした逸話的な報告が、神経障害性疼痛に対する大麻の有効性に関する科学的な調査を促進した側面があります。特に、カリフォルニア大学サンフランシスコ校で行われた研究では、大麻の喫煙摂取がHIV関連感覚神経障害の慢性神経障害性疼痛を軽減することが示されました。被験者らは、プラセボ群の17%に比べ、日々の痛みが34%軽減したと報告しており、大麻は耐容性が高く、効果的な痛みの緩和をもたらすことが示されたのです。
https://pubmed.ncbi.nlm.nih.gov/17296917/
HIV関連神経障害におけるこれらの研究の成功により、研究者たちはCIPNを含む他の神経障害性疼痛に対する大麻の潜在的可能性を探求するようになりました。神経障害のメカニズムはそれぞれの疾患で異なる可能性がありますが、エイズ患者で観察された大麻の鎮痛特性はCIPNの管理における大麻の使用を検討する上での基礎を提供しています。
本領域における処方箋医薬品開発を目指した早期の研究として、2014年にカナダのダルハウジー大学麻酔科に所属するメアリー・E・リンチ医師らの報告があります。研究チームはTHC: CBD=1:1で含有する製剤であるサティベックスを用いて、16名の CIPN患者を対象に疼痛改善効果を評価しました。参加者の癌の部位は、卵巣(5人)、子宮頸部(2人)、肺(1人)、子宮(1人)、乳房(3人)、血液(1人)、リンパ腫(1人)であり、参加者が受けた化学療法剤は、シスプラチン(3人)、オキサリプラチン(1人)、パクリタキセル(7人)、ビンクリスチン(1人)、併用療法(6人)でした。化学療法の平均サイクル数は5.72であり、痛みの平均持続期間は19か月でした。ベースラインでの平均NRS-PIスコアは6.78(標準偏差1.17)でした。この研究は全ての患者が実薬とプラセボの両方を投与される二重盲検クロスオーバー試験というデザインで行われました。サティベックス(もしくはプラセボ薬)の投与スケジュールは段階的に増量する方式であり、参加者は就寝前に舌下または頬の内側に1スプレーから開始するように指示されました。 その後、痛みが軽減されるまで、1日1〜2スプレーずつ薬剤を増やしていきました。最大用量は1日12スプレーで、なんらかの副作用が発生した場合は増量を中止するように指示されました。用量が確定したら、参加者はその用量を4週間維持し、2週間後と4週間後に再来院して効果指標の評価を受けました。最初の研究期間が終了したら、1日1〜2スプレーずつ薬剤を減らして中止し、2週間のウォッシュアウト期間を経て、2番目の研究薬剤を受けました。この試験の主要アウトカムは、ベースライン(治療前の7日間の平均疼痛スコア)と治療最終週の、痛みの強さを評価する11ポイントの数値評価スケール(NRS-PI)の変化でした。
試験の結果、グループ全体で見ると、サティベックス群とプラセボ群の間にNRS-PIに統計的に有意な差は認められませんでした。 しかしレスポンダー分析では、5人の参加者がNRS-PIで2ポイント以上の疼痛の減少を報告しており、これは統計的に有意な傾向を示しました。本研究から示唆される治療必要数(NNT)は5でした。これは、サティベックス治療を受けた5人の患者に対して、プラセボと比較して1人の患者が追加で臨床的に有意な疼痛の軽減を経験することを意味します。この結果は、神経障害性疼痛の治療に対する鎮痛剤の反応には、個人差が大きいことを示す文献と一致しています。 現在の神経障害性疼痛の標準治療薬のNNTにも幅広いばらつきがあり、最も効果的な鎮痛剤でもNNTは2.1(三環系抗うつ薬)および2.6(オピオイド)です。 この小規模な予備試験におけるサティベックスのNNTは5.0であり、これは現在神経障害性疼痛の治療に日常的に使用されている他の多くの薬剤と同様の範囲にあります。これらの結果から、サティベックスは化学療法誘発性神経障害性疼痛の治療薬として有望である可能性が示唆されました。
参考:
A double-blind, placebo-controlled, crossover pilot trial with extension using an oral mucosal cannabinoid extract for treatment of chemotherapy-induced neuropathic pain
106: https://pubmed.ncbi.nlm.nih.gov/23742737/
これら初期の臨床研究成果はCIPN治療薬としての大麻の可能性を示すものでしたが、2020年に米国臨床腫瘍学会が作成した成人のがん生存者における化学療法誘発性末梢神経障害の予防と管理に関するガイドラインでは、”経口カンナビノイド”は十分なエビデンスがなく現時点では推奨できないと判断されています。(大麻の喫煙摂取に対しては言及がありません)
https://ascopubs.org/doi/10.1200/JCO.20.01399
しかしそれ以降の5年間で、新たな研究が実施され知見は蓄積されつつあります。
2021年にはイスラエルのテルアビブ・ソウラスキー医療センター腫瘍内科の研究者であるWaissengrinらが、オキサリプラチン投与に伴う末梢神経障害に対する大麻の効果を後ろ向きに調査し報告しました。著者らは同センターで、2015年10月から2018年1月までに、5-フルオロウラシル(5FU)とオキサリプラチン併用療法を受けた消化管がん患者768名の医療記録をレビューしました。この研究では、大麻の使用と神経障害のグレード、オキサリプラチンの累積投与量、神経障害のない生存期間との関連性を調査しました。患者を大麻の使用状況に基づいて3つのグループに分けました。
①大麻先行群: オキサリプラチン投与前に大麻を使用していた患者(吐き気、食欲不振、疼痛、気分障害などのさまざまな症状に対してカンnabisが処方されていました)
②オキサリプラチン先行群: 大麻治療前にオキサリプラチン治療を受けた患者
③コントロール群: オキサリプラチン治療中に大麻を使用しなかった患者
その結果、大麻を使用していた患者群では、コントロール群と比較して、グレード2~3の神経障害の発症率が有意に低いことが明らかになりました(それぞれ15.3%と27.9%、p<0.001)。また①の大麻先行群では、②のオキサリプラチン先行群と比較して、神経障害の抑制効果がより顕著でした(それぞれ75%と46.2%、p<0.001)。加えて①大麻先行群では、②オキサリプラチン先行群およびコントロール群と比較して、オキサリプラチンの累積投与量が有意に高いことが明らかになりました(それぞれ545mg/m2、340mg/m2、425mg/m2、p<0.001)。これは大麻の副作用予防効果によって抗がん剤治療への認容性が高まった可能性を示唆しています。
この研究の結果は、オキサリプラチン治療を受ける消化管がん患者において、大麻の併用が神経障害の発症率を低下させる可能性があることを示唆しています。特に、オキサリプラチン治療前に大麻を予防的に使用した場合、神経障害に対する保護効果がより顕著である可能性があります。ただし、この研究は後ろ向き研究であるため、大麻の神経障害に対する保護効果を確定するためには、さらなる前向き研究が必要です。
https://pubmed.ncbi.nlm.nih.gov/33613702/
2021年にはアメリカ・Mayo ClinicのStacyらもこの領域におけるケースシリーズを報告しています。https://journals.sagepub.com/doi/full/10.1177/15347354211061739
この研究では2019年4月から2020年12月にかけて、カリフォルニア州サッター・メディカルグループとミネソタ州ロチェスターのメイヨークリニックにおいて、腫瘍科クリニックでCIPNの患者を対象に、局所カンナビノイド塗布治療の使用経験についてインタビューを行いました。合計22名の患者が局所カンナビノイドによる治療の恩恵を受けたと報告し、その詳細は表1にまとめられています。 表1には、がんの種類、化学療法の種類、症状の部位、試みたが失敗した治療法、大麻の種類などの情報が含まれています。患者はヘンプ由来のCBD製品を小売店から、またCBDとTHCを含む製品はディスペンサリーから入手していました。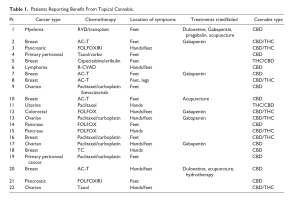
この論文では、局所カンナビノイドの使用により化学療法誘発性末梢神経障害(CIPN)の症状緩和がみられた患者の10症例の詳細を提示しています。以下は、各症例の詳細です。
症例1:49歳の男性で、2008年にレナリドミド、ボルテゾミブ、デキサメタゾン(RVD)による化学療法と自家骨髄移植を受けた多発性骨髄腫の患者さんです。治療後、足の重度の神経障害を発症し、活動が制限されました。ガバペンチン、プレガバリン、デュロキセチンを試しましたが、効果はありませんでした。2019年に鍼治療を開始しましたが、これも効果がありませんでした。関節炎の痛みや睡眠のために長年経口カンnabisを使用していましたが、CIPNには効果がありませんでした。1日1〜2回、CBDクリーム(250mg/瓶)の使用を開始し、神経障害性疼痛の有意な改善を報告しました。ベースラインの痛みを7〜10と評価していましたが、塗布後5分以内に4〜5/10に減少しました。効果は一晩中持続したと述べています。塗布時にわずかな熱感を感じましたが、痛みやその他の副作用はありませんでした。
症例2:73歳の女性で、2017年にステージIIの乳がんに対してドキソルビシン、シクロホスファミド、パクリタキセル(AC-T)による治療を受けた患者さんです。治療後、夜間に気になる足の神経障害を発症しました。ガバペンチンを試しましたが効果がなく、めまいを起こしました。地元の大麻薬局から入手したTHC/CBDクリーム(mg不明)の使用を開始しました。ベースラインの神経障害は8/10と評価されていましたが、塗布後数分以内に2〜3/10に改善しました。効果は一晩中持続し、副作用はなかったと報告しています。ガバペンチンを中止し大麻クリームの使用を継続し効果が持続しています。
症例3:65歳の男性で、オキサリプラチンベースの化学療法後にCIPNを発症した膵臓がんの患者さんです。足と手のベースラインの神経障害は6/10と評価されました。約600mgのCBDと600mgのTHCを含むクリームを使用していると報告しています。数日以内に塗布した後、症状は4/10に改善し、効果はほとんど一日中持続します。副作用なく毎日クリームを使い続けています。
症例4:71歳の女性で、タキサンベースの化学療法後に痛みを伴うCIPNを発症した原発性腹膜がんの患者さんです。 ベースラインの痛みは7/10と評価されました。CBDクリーム(250mg/瓶)を使用していると報告しており、塗布後数分以内に痛みが3/10に減少し約12時間持続します。 副作用なく毎日クリームを使用しています。
症例5:78歳の女性で、カペシタビン-エリブリン化学療法後にCIPNを発症した進行乳がんの患者さんです。ベースラインのCIPNは6/10と評価されていましたが、CBD 180mg/THC 6mg/瓶を含むクリームを塗布15分後に足の痛みが1/10に減少しました。 効果は24時間持続し、副作用は報告されていません。 毎日使用しています。
症例6:59歳の男性で、シクロホスファミド、ビンクリスチン、ドキソルビシン、デキサメタゾンによる治療後に足と手に重度のCIPNを発症したリンパ腫の患者さんです。 ベースラインの痛みを10/10と評価しています。CBDのみ200mg/瓶を含むクリームを使用しており、約30分後に5/10に改善したと報告しています。 効果は約3時間持続し、副作用はありません。
症例7:60歳の女性で、AC-T化学療法後にCIPNを発症した乳がんの患者さんです。ガバペンチンを服用しているにもかかわらず、夜間の足の痛みは8/10と評価されました。CBDクリーム(120mg/瓶)を使用しており、塗布後10〜15分以内に痛みが0/10に改善し、効果は一晩中持続したと述べています。このクリームには、吸収を促進するエッセンシャルオイルが含まれています。毎晩クリームを使用しており、副作用は報告されていません。
症例8:55歳の女性で、乳がんのAC-T化学療法(アドリアマイシン・シクロフォスファミド・タキソテール)後に足と脚にCIPNを発症した患者さんです。ベースラインのCIPNは6/10と評価されていましたが、477mgのTHCと158mgのCBD/瓶を含むクリームを使用することで1/10に改善しました。 10〜15分後に改善が見られ、効果は2〜3時間持続します。 週に数回、主に夜に使用しており、副作用なく睡眠に役立っています。
症例9:64歳の女性で、タキサンベースの化学療法後に痛みを伴うCIPNを発症した再発卵巣がんの患者さんです。ベースラインの足の痛みは6/10と評価されていましたがCBDオイル(250mg/瓶)を使用後4/10に改善しました。 オイルは10分で効果が現れ始め、効果は一晩中持続すると述べています。 毎晩使用し、時には朝にも塗布しますが、副作用は報告されていません。
症例10:62歳の女性で、AC-T化学療法により足の神経障害を発症した乳がんの患者さんです。 鍼治療を試みましたが効果はありませんでした。ベースラインの神経障害は8/10と評価されていましたがCBDクリーム(mg不明)を使用後10分で5/10に改善し、効果は約3時間持続しました。 1日2回クリームを使用しており、副作用はありません。
これらの10症例は表1の最初の10症例として要約されており、さらに12症例の要約が続いています。
2022年にはデンマーク・ジーランド大学の研究者によるCBDの前投与がCIPNを予防するかどうかの介入試験結果が報告されています。今回対象となった抗がん剤のレジメンはカルボプラチン+パクリタキセル療法(TC)と カペシタビン+オキサリプラチン療法(CAPOX)でした。TCは非小細胞肺がんや卵巣がんの治療レジメンとして活用され、どちらの薬剤も点滴で短回投与されました。CAPOXは主に大腸がんの治療レジメンで、オキサリプラチンの単回点滴投与とカペシタビンの14日間の内服を実施しました。CBDを服用する患者群(54名)は、抗がん剤投与開始の前日からCBD300mg/day(一日2回)を服用開始し、8日間毎日内服しました。使用されたCBDはGlostrup Pharmacy社によって製造されたGMP基準を満たすティンクチャー(10%)、THCの含有量は0.01%以下であり、0.2%のCBDVと0.1%のCBD-C4という成分を含有していました。急性の神経障害については、この研究のために用意した10項目からなる自覚症状スコア(それぞれ10点満点で点数が高いほど症状が悪い)と、特別な測定機器(VibroSense Meter Ⅱ)を用いた客観的な評価を実施しました。するとCAPOX患者では10項目のうち4項目(冷覚の低下・冷水を飲み込んだ際の違和感・咽頭不快感・精密運動のやりづらさ)でCBD投与群で有意に症状の低下を認めました。TC療法では1項目(最小の痛み)だけが有意な改善を認めました。計測機器を用いた評価でも同様の傾向が示されました。
Oral cannabidiol for prevention of acute and transient chemotherapy-induced peripheral neuropathy. https://link.springer.com/article/10.1007/s00520-022-07312-y
2024年にはアメリカのメイヨークリニックの研究チームがCBD塗布薬を用いた臨床試験の結果を報告しています。この研究では、CIPNと確定された40名の患者を対象に、CBD単離物(アイソレート)を含むクリームとプラセボ(偽薬)クリームを2週間ずつ塗布するクロスオーバー試験が行われました。患者はどちらのクリームを先に使用するか無作為に割り付けられ、研究者も患者もどちらのクリームを使用しているかわからない二重盲検で行われました。主要評価項目は、ベースラインから2週間後のEORTC-QLQ-CIPN20という質問票の感覚神経障害サブスケールの変化でした。副次評価項目には、運動神経障害や自律神経障害の評価、CIPNAT、Global Impression of Change tool、NCI-CTCAE神経障害スケールなどが含まれました。また、症状日記を用いて副作用も記録されました。CBDクリームは、1.7オンス(48g)あたり250mgのCBDアイソレートを含んでおり(0.5%)、THCは含まれていませんでした。患者は、影響を受けている部位(手や足)に、1日2回、約4mgのCBDを含むクリームを塗布するよう指示されました。
研究の結果、CBDクリーム群とプラセボ群の間で、主要評価項目であるEORTC-CIPN20感覚神経障害スコアに有意な差は見られませんでした。同様に、他の神経障害の評価項目や毒性スコアにおいても、両群間で有意な差は見られませんでした。ただし、最初の2週間の試験期間において、CBDクリームを使用した患者群で、立ちくらみ(自律神経症状の1項目)の改善がわずかに見られました。また、CIPNATを用いた評価では、CBD群で書字、家事、着替え、仕事における支障の改善が報告されましたが、プラセボ群へのクロスオーバー後も持続したため、偶然による可能性が高いと結論付けられました。副作用については、全体的にCBDクリームは良好な忍容性を示し、重篤な副作用は報告されませんでした。
このパイロット試験の結果から、研究されたCBDアイソレートクリームは、確立された痛みを伴うCIPNの症状を改善するという明確な証拠は得られませんでした。しかし、忍容性は良好であることが示されました。研究者らは、今後の研究として、フルスペクトラムのカンナビス抽出物や、より高濃度のCBDを用いた試験の可能性を示唆しています。また、プラセボ効果の可能性も考慮し、プラセボ対照試験の重要性を強調しています。今回の研究では明確な効果は示されませんでしたが、CBDとCIPNに関する研究はまだ始まったばかりです。今後の研究の進展に注目していきましょう。
https://pubmed.ncbi.nlm.nih.gov/39016024/
参考:総説(2024)Chemotherapy-Induced Peripheral Neuropathy: A Recent Update on Pathophysiology and Treatment.
https://www.mdpi.com/2075-1729/14/8/991
更新日:2025年4月18日
執筆:正高佑志 Yuji Masataka(医師) 経歴: 2012年医師免許取得。2017-2019年熊本大学脳神経内科学教室所属。2025年聖マリアンナ医科大学・臨床登録医。 研究分野:臨床カンナビノイド医学 活動: 2017年に一般社団法人Green Zone Japanを設立し代表理事に就任。独自の研究と啓発活動を継続している。令和6年度厚生労働特別研究班(カンナビノイド医薬品と製品の薬事監視)分担研究者。 書籍: お医者さんがする大麻とCBDの話(彩図社)、CBDの教科書(ビオマガジン) 所属学会: 日本内科学会、日本臨床カンナビノイド学会(副理事長)、日本てんかん学会(評議員)、日本アルコールアディクション医学会(評議員)
コメントを残す